
تتم مراجعة جميع محتويات iLive طبياً أو التحقق من حقيقة الأمر لضمان أكبر قدر ممكن من الدقة الواقعية.
لدينا إرشادات صارمة من مصادرنا ونربط فقط بمواقع الوسائط ذات السمعة الطيبة ، ومؤسسات البحوث الأكاديمية ، وطبياً ، كلما أمكن ذلك استعراض الأقران الدراسات. لاحظ أن الأرقام الموجودة بين قوسين ([1] و [2] وما إلى ذلك) هي روابط قابلة للنقر على هذه الدراسات.
إذا كنت تشعر أن أيًا من المحتوى لدينا غير دقيق أو قديم. خلاف ذلك مشكوك فيه ، يرجى تحديده واضغط على Ctrl + Enter.
عقار LM11A-31 يبطئ من تطور مرض الزهايمر في التجربة
آخر مراجعة: 02.07.2025

في دراسة حديثة نشرت في مجلة Nature Medicine ، أجرى العلماء دراسة عشوائية مزدوجة التعمية وخاضعة للتحكم الوهمي من المرحلة 2أ لفحص سلامة وفعالية LM11A-31 في علاج مرض الزهايمر (AD) من خلال تعديل مستقبلات p75 العصبية (p75NTR).
يُعدّ مرض الزهايمر المتأخر الظهور أكثر أشكال الخرف شيوعًا، ويتميز بفشل التشابك العصبي، والتنكس، وفقدان الخلايا العصبية. على الرغم من أن العقارين الرئيسيين لعلاج الزهايمر يستهدفان تراكم بروتينات بيتا أميلويد أو تاو غير الطبيعية، إلا أنهما لا يعالجان سوى جزء من الفيزيولوجيا المرضية. يتضمن نهج آخر استهداف المستقبلات وشبكات الإشارات التي تؤثر على المسارات البيولوجية الأساسية. تُظهر الدراسات ما قبل السريرية أن تعديل p75NTR باستخدام جزيء كيميائي صغير جديد، LM11A-31، يقلل من فقدان التشابك العصبي الناتج عن بروتينات بيتا أميلويد وتاو غير الطبيعية.
وصف الدراسة
في هذه التجربة السريرية العشوائية، فحص الباحثون ما إذا كان LM11A-31 قادرًا على إبطاء تقدم مرض الزهايمر عن طريق تعديل p75NTR في البشر.
أُعطي المشاركون في الدراسة كبسولات LM11A-31 الفموية بجرعات 200 ملغ و400 ملغ، أو دواءً وهميًا بنسبة 1:1:1، لـ 242 مريضًا يعانون من ربو خفيف إلى متوسط لمدة 26 أسبوعًا. شُخِّصَت إصابة المشاركين بمرض الزهايمر (مستوى بروتين بيتا أميلويد 42 في السائل النخاعي (Aβ42) أقل من 550 نانوغرام/لتر، أو نسبة Aβ42:β40 أقل من 0.89) وفقًا لمعايير ماكهان، مع درجات تتراوح بين 18 و26 في الفحص النفسي المصغر (MMSE)، ودرجات أقل من 5.0 في مقياس الاكتئاب الشيخوخي (GDS)، ودرجات أقل من 4.0 في مقياس هاشينسكي الإقفاري المُعَدَّل (HIS)، وعمرهم 8 سنوات أو أكثر، وتدهور إدراكي سابق لمدة 6 أشهر أو أكثر.
تناول المشاركون المؤهلون مثبطات الأسيتيل كولينستراز (AChEIs) أو مضادات مستقبلات NMDA الجزئية لمدة 3 أشهر أو أكثر قبل بدء الدراسة. ولم يتناولوا أي أدوية غير مشروعة، مثل مضادات الذهان، والبنزوديازيبينات، ومضادات الصرع، والمهدئات، وخافضات ضغط الدم المركزية، والمنشطات الذهنية (باستثناء الجنكة بيلوبا)، أو المسكنات المحتوية على المواد الأفيونية.
كانت النتيجة الرئيسية للدراسة هي السلامة والتحمل، وقد تم تقييمها باستخدام مقياس كولومبيا لشدة الأفكار والسلوك الانتحاري (C-SSRS)، والعلامات الحيوية، وضغط الدم، والمعايير الدموية. واستُخدمت التصوير بالرنين المغناطيسي الهيكلي (cMRI)، والتصوير المقطعي بالإصدار البوزيتروني بالفلوروديوكسي جلوكوز (FDG-PET)، والمؤشرات الحيوية للسائل النخاعي (CSF) لتقييم النتائج المعرفية الثانوية. وشملت مقاييس AD بروتين تاو المفسفر بواسطة Thr181، وبروتين تاو الكلي، وAβ40، وAβ42، ونشاط AChE. واستخدم الفريق اختبارًا نفسيًا عصبيًا مُخصصًا لتقييم النتائج المعرفية الثانوية في بداية الدراسة، وفي الأسبوعين 12 و26.
نتائج البحث
وجدت الدراسة أن LM11A-31 آمن وجيد التحمل، ولا توجد أي مخاوف كبيرة تتعلق بالسلامة. وشملت الآثار الجانبية الأكثر شيوعًا الصداع، والإسهال، وفرط الحمضات، والتهاب البلعوم الأنفي، وكانت مشاكل الجهاز الهضمي وفرط الحمضات السببين الرئيسيين للتوقف عن العلاج. كان هناك عدد أكبر من حالات التوقف عن العلاج في مجموعة جرعة 400 ملغ مقارنةً بمجموعتي جرعة 200 ملغ والدواء الوهمي. ولم يكشف التصوير بالرنين المغناطيسي عن أي مخاوف تتعلق بالسلامة، بما في ذلك أي تشوهات مرتبطة بالأميلويد. ولم تُلاحظ أي فروق جوهرية في الدرجات الإدراكية أو أي تشوهات أميلويد بين مجموعتي العلاج.
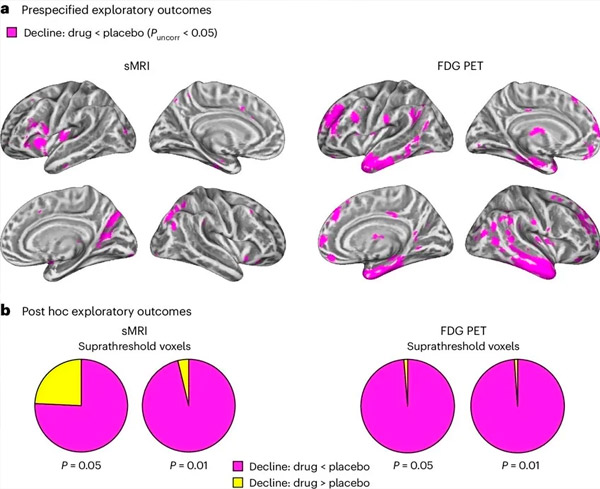
أ. حلل تحليل التباين ثنائي الاتجاه للنماذج المختلطة التفاعلات بين العلاج (دواء أو دواء وهمي) والوقت (قبل العلاج أو بعده). أظهر تباين t أحادي الطرف، الذي فحص فرضية التفاعل (الدواء يُبطئ التقدم مقارنةً بالدواء الوهمي)، أن علاج LM11A-31 أبطأ التنكس الطولي (اللوحات اليسرى) وقصور أيض الجلوكوز (اللوحات اليمنى) في مجموعة الدواء (تصوير بالرنين المغناطيسي، عدد = 127؛ تصوير بالإصدار البوزيتروني، عدد = 121) مقارنةً بمجموعة الدواء الوهمي (تصوير بالرنين المغناطيسي، عدد = 66؛ تصوير بالإصدار البوزيتروني، عدد = 62). تظهر وحدات فوكسل التي تُظهر هذا التفاعل عند عتبة غير مصححة P < 0.05 (أرجواني) على سطح قشري خاص بالسكان. يظهر نصفا الكرة المخية الأيسر والأيمن في الصفين العلوي والسفلي على التوالي. تظهر مناطق الدماغ التي تُظهر تفاعلات لا تتوافق مع الفرضية في الشكل 7 في البيانات التكميلية.
ب. العدد الإجمالي للفوكسلات في مناطق الدماغ المعرضة للإصابة بمرض الزهايمر المحددة مسبقًا (المساحة الكلية للمخططات الدائرية) التي تُظهر إما تفاعلًا متوافقًا مع الفرضية (أرجواني) أو تفاعلًا غير متوافق معها (أصفر) في كلٍّ من تقنيتي التصوير (التصوير بالرنين المغناطيسي الوظيفي، اللوحة اليسرى؛ التصوير بالبوزيترون بالفلورو جلوكوز، اللوحة اليمنى) عند عتبات متزايدة التفاوت من قيمة P < 0.01 وقيمة P < 0.05 غير المصححة. أظهرت محاكاة مونت كارلو أن نسب الفوكسلات التي تُظهر تأثيرات متوافقة مع الفرضية مقابل تلك التي لا تتوافق معها كانت أعلى بكثير من تلك التي لوحظت بناءً على بيانات مُولّدة عشوائيًا لكلٍّ من التصوير بالرنين المغناطيسي الوظيفي والتصوير بالبوزيترون بالفلورو جلوكوز (قيمة P < 0.001 لكل تقنية؛ اختبار ثنائي الذيل).
قلّل LM11A-31 بشكل فعال من زيادة مستويات Aβ42 وAβ40 في السائل الدماغي الشوكي مقارنةً بمجموعة الدواء الوهمي. كما أظهر الدواء انخفاضًا في متوسط النسبة المئوية السنوية للتغير في المؤشر الحيوي للبروتين قبل المشبكي SNAP25، وانخفاضًا في المؤشر الحيوي بعد المشبكي NG، مما يشير إلى تباطؤ فقدان الوصلات قبل المشبكية وبعد المشبكية. كما قلّل LM11A-31 من زيادة YKL40، مما أدى إلى انخفاض في درجات MMSE وزيادة في درجات ADAS-Cog-13. كما قلّل الدواء من فقدان المادة الرمادية في الفص الجبهي والقشرة الجدارية الخلفية، وانخفاضًا في استقلاب الجلوكوز في مناطق مثل القشرة الشمية الداخلية، والقشرة الصدغية، والحُصين، والقشرة الجزيرية، والقشرة الجبهية.
خاتمة
خلصت الدراسة إلى أن تعديل p75NTR بواسطة LM11A-31 مناسب للتجارب السريرية الأوسع. وقد حقق LM11A-31 نقطة النهاية الأساسية للسلامة، وكان جيد التحمل لدى مرضى الزهايمر الذين تتراوح حالاتهم بين الخفيفة والشديدة. تشير النتائج إلى الحاجة إلى مزيد من الدراسات ذات فترات علاج أطول لتقييم قدرة الجزيئات الصغيرة على تنظيم p75NTR كعلاج معدِّل للمرض في الزهايمر. أظهرت الدراسة أن LM11A-31 أثر بشكل ملحوظ على العديد من المؤشرات الحيوية، بما في ذلك Aβ40 وAβ42 وSNAP25 وNG وYKL40، مما يشير إلى تباطؤ التقدم المرضي. قد تُقيّم الدراسات المستقبلية مؤشرات إضافية لصحة الخلايا الدبقية.
