
تتم مراجعة جميع محتويات iLive طبياً أو التحقق من حقيقة الأمر لضمان أكبر قدر ممكن من الدقة الواقعية.
لدينا إرشادات صارمة من مصادرنا ونربط فقط بمواقع الوسائط ذات السمعة الطيبة ، ومؤسسات البحوث الأكاديمية ، وطبياً ، كلما أمكن ذلك استعراض الأقران الدراسات. لاحظ أن الأرقام الموجودة بين قوسين ([1] و [2] وما إلى ذلك) هي روابط قابلة للنقر على هذه الدراسات.
إذا كنت تشعر أن أيًا من المحتوى لدينا غير دقيق أو قديم. خلاف ذلك مشكوك فيه ، يرجى تحديده واضغط على Ctrl + Enter.
تم ابتكار لقاح اصطناعي معقد يعتمد على جزيئات الحمض النووي
خبير طبي في المقال
آخر مراجعة: 01.07.2025
في البحث عن طرق لإنشاء لقاحات أكثر أمانًا وفعالية، لجأ العلماء في معهد التصميم الحيوي بجامعة ولاية أريزونا إلى مجال واعد يسمى تقنية النانو للحمض النووي لإنشاء نوع جديد تمامًا من اللقاحات الاصطناعية.
في دراسة نشرت مؤخرا في مجلة Nano Letters، تعاون عالم المناعة يونج تشانج من معهد الهندسة الحيوية مع زملاء من بينهم خبير تكنولوجيا النانو في الحمض النووي الشهير هاو يان لتركيب أول مجمع لقاح في العالم يمكن توصيله بأمان وكفاءة إلى مواقع مستهدفة من خلال وضعه على هياكل نانوية ثلاثية الأبعاد للحمض النووي ذاتية التجميع.
يقول تشانغ، الأستاذ المشارك في كلية علوم الحياة والباحث في مركز الأمراض المعدية واللقاحات بمعهد الهندسة الحيوية: "عندما اقترح هاو اعتبار الحمض النووي منصةً عمليةً لا مادةً وراثية، خطرت لي فكرة تطبيق هذا النهج على علم المناعة. وهذا من شأنه أن يتيح لنا فرصةً عظيمةً لاستخدام حاملات الحمض النووي لإنتاج لقاحٍ اصطناعي".
كان السؤال الأهم: هل هو آمن؟ أردنا ابتكار مجموعة من الجزيئات القادرة على تحفيز استجابة مناعية آمنة وقوية في الجسم. وبما أن فريق هاو دأب على تصميم هياكل نانوية مختلفة للحمض النووي على مدى السنوات القليلة الماضية، فقد بدأنا التعاون لإيجاد تطبيقات طبية محتملة لهذه الهياكل.
وتتمثل خصوصية الطريقة التي اقترحها العلماء من ولاية أريزونا في أن حامل المستضد هو جزيء الحمض النووي.
وضم فريق البحث متعدد التخصصات أيضًا طالب الدراسات العليا في الكيمياء الحيوية بجامعة أريزونا والمؤلف الأول للورقة البحثية شياووي ليو، والأستاذ يانغ شو، ومحاضر الكيمياء الحيوية يان ليو، وطالب كلية العلوم البيولوجية كريج كليفورد، وتاو يو، طالب الدراسات العليا من جامعة سيتشوان في الصين.
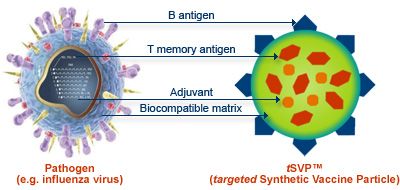
يشير تشانغ إلى أن الانتشار الواسع للتطعيمات أدى إلى أحد أهم إنجازات الصحة العامة. يعتمد فن إنتاج اللقاحات على الهندسة الوراثية لبناء جزيئات شبيهة بالفيروسات من بروتينات تُحفز الجهاز المناعي. تشبه هذه الجزيئات في بنيتها الفيروسات الحقيقية، لكنها لا تحتوي على مكونات وراثية خطيرة تُسبب الأمراض.
إن إحدى المزايا المهمة لتكنولوجيا النانو للحمض النووي، والتي تسمح بإعطاء الجزيء الحيوي شكلًا ثنائيًا أو ثلاثي الأبعاد، هي القدرة على إنشاء جزيئات باستخدام طرق دقيقة للغاية يمكنها أداء وظائف نموذجية للجزيئات الطبيعية في الجسم.
يوضح يانغ، مدير قسم الكيمياء والكيمياء الحيوية والباحث في مركز الفيزياء الحيوية للجزيئات المفردة بمعهد الهندسة الحيوية: "أجرينا تجارب على أحجام وأشكال مختلفة من هياكل الحمض النووي النانوية، وأضفنا إليها جزيئات حيوية لمعرفة كيفية استجابة الجسم لها". ومن خلال نهج يُطلق عليه العلماء "المحاكاة الحيوية"، تُقارب مُركّبات اللقاحات التي اختبروها حجم وشكل جزيئات الفيروس الطبيعية.
ولإثبات جدوى مفهومهم، قام الباحثون بربط بروتين تحفيز المناعة ستربتافيدين (STV) ودواء تعزيز المناعة أوليجوديوكسي نيوكليوتيد CpG بهياكل منفصلة من الحمض النووي المتفرعة على شكل هرمي، وهو ما يسمح لهم في نهاية المطاف بالحصول على مركب لقاح اصطناعي.
احتاج الفريق أولًا إلى إثبات قدرة الخلايا المستهدفة على امتصاص البنى النانوية. وبربط جزيء وسم باعث للضوء بالبنية النانوية، تمكن العلماء من التحقق من أن البنية النانوية وجدت مكانها الصحيح في الخلية وظلت مستقرة لعدة ساعات، وهي مدة كافية لتحفيز استجابة مناعية.
بعد ذلك، في تجارب أُجريت على الفئران، عمل العلماء على إيصال "حمولة" اللقاح إلى الخلايا التي تُمثل الحلقات الأولى في سلسلة الاستجابة المناعية للجسم، مُنسِّقين التفاعلات بين مختلف المكونات، مثل الخلايا المُقدِّمة للمستضد، بما في ذلك الخلايا البلعمية والخلايا الشجيرية والخلايا البائية. بمجرد دخول البنى النانوية إلى الخلية، تُحلَّل وتُعرَض على سطحها لتتعرف عليها الخلايا التائية، وهي خلايا الدم البيضاء التي تلعب دورًا محوريًا في تحفيز الاستجابة الدفاعية للجسم. بدورها، تُساعد الخلايا التائية الخلايا البائية على إنتاج أجسام مضادة للمستضدات الغريبة.
لاختبار جميع المتغيرات بشكل موثوق، قام الباحثون بحقن الخلايا بكل من مجمع اللقاح الكامل ومستضد STV وحده، بالإضافة إلى مستضد STV المخلوط مع معزز CpG.
بعد فترة 70 يومًا، وجد العلماء أن الفئران المُحصَّنة بمركب اللقاح الكامل أظهرت استجابة مناعية أقوى بتسعة أضعاف من تلك المُحفَّزة بمزيج CpG/STV. وكان التفاعل الأبرز هو الذي بدأه الهيكل رباعي السطوح (الهرمي). ومع ذلك، لم تُعرَف الاستجابة المناعية لمركب اللقاح على أنها نوعية (أي رد فعل الجسم تجاه مستضد محدد استخدمه الباحثون) وفعالة فحسب، بل وثبتت سلامتها أيضًا، وهو ما يؤكده غياب أي رد فعل مناعي تجاه الحمض النووي "الفارغ" (غير الحامل للجزيئات الحيوية) المُدخَل إلى الخلايا.
يقول تشانغ: "كنا سعداء للغاية. كان من الرائع رؤية النتائج التي توقعناها. هذا أمر نادر في علم الأحياء".
مستقبل صناعة الأدوية يكمن في الأدوية المستهدفة
يدرس الفريق حاليًا إمكانية تطوير طريقة جديدة لتحفيز خلايا مناعية محددة لتحفيز استجابة باستخدام منصة الحمض النووي. يمكن استخدام هذه التقنية الجديدة لتطوير لقاحات تتكون من عدة أدوية فعالة، بالإضافة إلى تغيير الأهداف لتنظيم الاستجابة المناعية.
وبالإضافة إلى ذلك، تتمتع التكنولوجيا الجديدة بالقدرة على تطوير أساليب جديدة للعلاج المستهدف، وخاصة إنتاج الأدوية "المستهدفة" التي يتم توصيلها إلى مناطق محددة بدقة من الجسم وبالتالي لا تنتج آثارًا جانبية خطيرة.
وأخيرا، ورغم أن مجال الحمض النووي لا يزال في مراحله الأولى، فإن العمل العلمي الذي يقوم به الباحثون في أريزونا له آثار عملية كبيرة على الطب والإلكترونيات وغيرها من المجالات.
يُقرّ تشانغ ويانغ بأنه لا يزال هناك الكثير مما يجب تعلمه وتحسينه بشأن طريقة اللقاح التي ابتكراها، لكن قيمة اكتشافهما لا تُنكر. ويختتم تشانغ قائلاً: "مع إثبات المفهوم، يُمكننا الآن إنتاج لقاحات مُركّبة بعدد غير محدود من المستضدات".
تم توفير الدعم المالي لهذا البحث من قبل وزارة الدفاع الأمريكية والمعاهد الوطنية للصحة.
 [ 1 ]، [ 2 ]، [ 3 ]، [ 4 ]، [ 5 ]، [ 6 ]، [ 7 ]، [ 8 ]، [ 9 ]
[ 1 ]، [ 2 ]، [ 3 ]، [ 4 ]، [ 5 ]، [ 6 ]، [ 7 ]، [ 8 ]، [ 9 ]

