منشورات جديدة
جهاز جديد يحسن توليد الخلايا الجذعية لعلاج الزهايمر
آخر مراجعة: 02.07.2025

تتم مراجعة جميع محتويات iLive طبياً أو التحقق من حقيقة الأمر لضمان أكبر قدر ممكن من الدقة الواقعية.
لدينا إرشادات صارمة من مصادرنا ونربط فقط بمواقع الوسائط ذات السمعة الطيبة ، ومؤسسات البحوث الأكاديمية ، وطبياً ، كلما أمكن ذلك استعراض الأقران الدراسات. لاحظ أن الأرقام الموجودة بين قوسين ([1] و [2] وما إلى ذلك) هي روابط قابلة للنقر على هذه الدراسات.
إذا كنت تشعر أن أيًا من المحتوى لدينا غير دقيق أو قديم. خلاف ذلك مشكوك فيه ، يرجى تحديده واضغط على Ctrl + Enter.

يقول باحثون في السويد إنهم نجحوا في إتقان تقنية لتحويل خلايا الجلد العادية إلى خلايا جذعية عصبية، الأمر الذي يقولون إنه يقربهم من العلاجات الخلوية الشخصية بأسعار معقولة لمرض الزهايمر ومرضباركنسون.
باستخدام جهاز ميكروسيال مصمم خصيصًا، طور فريق البحث نهجًا غير مسبوق ومتسارع لإعادة برمجة خلايا الجلد البشرية إلى خلايا جذعية متعددة القدرات (iPSCs) ثم تحويلها إلى خلايا جذعية عصبية.
تقول سوميا جين، المؤلفة الرئيسية للدراسة، إن المنصة قد تُحسّن وتُخفّض تكلفة العلاج الخلوي من خلال جعل الخلايا أكثر توافقًا وتقبلًا لجسم المريض. نُشرت الدراسة في مجلة "أدفانسد ساينس" من قِبل علماء من المعهد الملكي للتكنولوجيا في كيه تي إتش.
وقالت آنا هيرلاند، المؤلفة الرئيسية للدراسة، إن الدراسة أظهرت أول استخدام للتقنيات الدقيقة لتوجيه الخلايا الجذعية متعددة القدرات لتصبح خلايا جذعية عصبية.
خلايا جذعية عصبية متمايزة باستخدام منصة ميكروفلويدية. الصورة: المعهد الملكي للتكنولوجيا KTH
في الواقع، تتم عملية تحويل الخلايا الطبيعية إلى خلايا جذعية عصبية على مرحلتين. أولاً، تتعرض الخلايا لإشارات كيميائية حيوية تحفزها على التحول إلى خلايا جذعية متعددة القدرات (iPSCs)، قادرة على توليد أنواع مختلفة من الخلايا.
ثم تُنقل إلى بيئة تُحاكي الإشارات والعمليات التنموية المُشاركة في تكوين الجهاز العصبي. تُعيد هذه الخطوة، التي تُسمى التمايز العصبي، توجيه الخلايا لتصبح خلايا جذعية عصبية.
على مدار العقد الماضي، تحولت بيئة المختبر لهذا النوع من العمل تدريجيًا من الأجهزة اللوحية التقليدية إلى الأجهزة الدقيقة. ويقول هيرلاند إن المنصة الجديدة تُمثل تحسنًا في مجال الموائع الدقيقة في مرحلتي توليد الخلايا الجذعية متعددة القدرات وتمايز الخلايا الجذعية العصبية.
وباستخدام خلايا من خزعات الجلد البشري، وجد الباحثون أن المنصة الميكروفلويدية تعمل على تسريع التزام الخلايا بمصير عصبي في مرحلة مبكرة مقارنة بتلك المتمايزة في الألواح التقليدية.
ويقول هيرلاند: "لقد وثقنا أن البيئة المحصورة لمنصة الميكروفلويديك تعزز الالتزام بتوليد الخلايا الجذعية العصبية".
صورة مقربة لرقاقة الموائع الدقيقة المستخدمة لتحفيز الخلايا الجذعية. الصورة: المعهد الملكي للتكنولوجيا KTH
ويقول جين إن الشريحة الميكروسيالية من السهل تصنيعها باستخدام بولي دايميثيل السيلوكسان (PDMS)، كما أن حجمها المجهري يسمح بتحقيق وفورات كبيرة في الكواشف ومواد الخلايا.
ويضيف أنه يمكن تعديل المنصة بسهولة لاستيعاب التمايز إلى أنواع أخرى من الخلايا. ويمكن أتمتتها، مما يوفر نظامًا مغلقًا يضمن الاتساق والموثوقية في إنتاج مجموعات خلايا متجانسة للغاية.
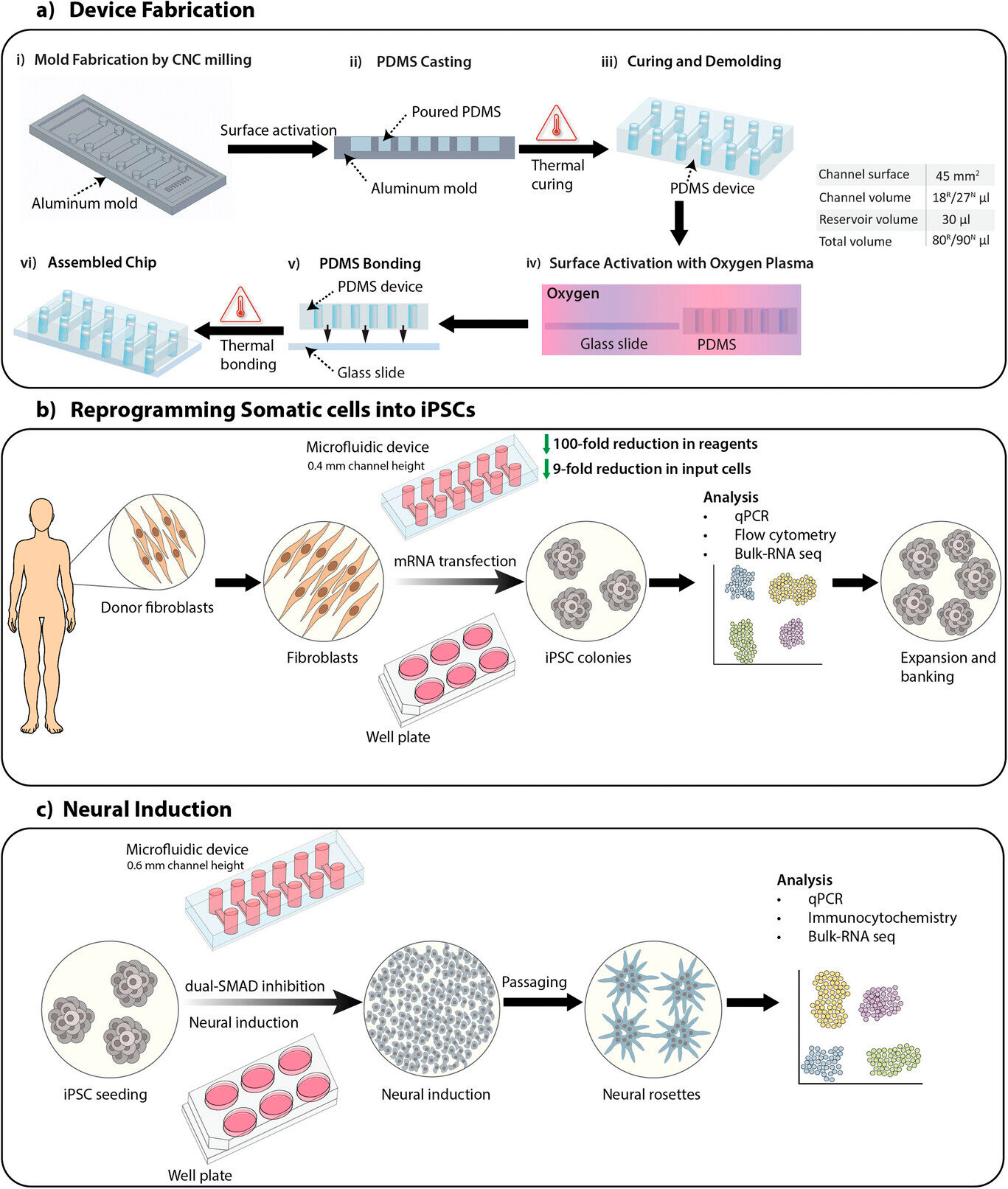
نظرة عامة على الدراسة، بما في ذلك تصنيع الجهاز، وإعادة برمجة الخلايا الجسدية إلى خلايا جذعية متعددة القدرات مُستحثة (iPSCs)، والتحفيز العصبي لهذه الخلايا باستخدام بروتوكول التثبيط المزدوج SMAD لتوليد الخلايا الجذعية العصبية.
أ) عملية تصنيع جهاز ميكروفلويدي بقنوات بارتفاع 0.4 مم و0.6 مم لإعادة برمجة الخلايا الجسدية (R) والتحفيز العصبي (N)، على التوالي. أحجام القنوات والحجم الإجمالي مُدرجة في الجدول.
ب) نظرة عامة على عملية إعادة برمجة الخلايا الجسدية إلى خلايا جذعية متعددة القدرات مُستحثة على أجهزة وصفائح ميكروفلويدية باستخدام نقل الرنا المرسال (mRNA).
ج) نظرة عامة على عملية التحفيز العصبي للخلايا iPSCs إلى خلايا جذعية عصبية على أجهزة وصفائح ميكروفلويدية باستخدام بروتوكول التثبيط المزدوج SMAD.
المصدر: Advanced Science (2024). DOI: 10.1002/advs.202401859
ويضيف جين: "هذه خطوة نحو جعل العلاجات الخلوية المخصصة لمرض الزهايمر ومرض باركنسون في متناول الجميع".
وشارك في الدراسة أيضًا علماء من معهد كارولينسكا وجامعة لوند، بالتعاون مع اتحاد IndiCell.
