
تتم مراجعة جميع محتويات iLive طبياً أو التحقق من حقيقة الأمر لضمان أكبر قدر ممكن من الدقة الواقعية.
لدينا إرشادات صارمة من مصادرنا ونربط فقط بمواقع الوسائط ذات السمعة الطيبة ، ومؤسسات البحوث الأكاديمية ، وطبياً ، كلما أمكن ذلك استعراض الأقران الدراسات. لاحظ أن الأرقام الموجودة بين قوسين ([1] و [2] وما إلى ذلك) هي روابط قابلة للنقر على هذه الدراسات.
إذا كنت تشعر أن أيًا من المحتوى لدينا غير دقيق أو قديم. خلاف ذلك مشكوك فيه ، يرجى تحديده واضغط على Ctrl + Enter.
دعامة عصبية للجهاز الهضمي: تعيد الحركة الدودية وتنشط "هرمونات الشبع"
آخر مراجعة: 18.08.2025
 ">
">تُصيب اضطرابات حركة الجهاز الهضمي (المريء والمعدة) - مثل تعذر الارتخاء، وشلل المعدة، وعسر البلع، وغيرها - أكثر من 20% من السكان، وتُسبب معدلات مرضية وتكاليف باهظة. غالبًا ما تكون فعالية الأساليب العلاجية التقليدية - مثل الأدوية والتدخلات السلوكية والجراحة - محدودة، ولا تُعيد الحركة الدودية الطبيعية.
- لماذا لا تحل الأجهزة الحالية المشكلة؟ دُرِس التحفيز الكهربائي للجهاز الهضمي منذ ستينيات القرن الماضي، لكن الغرسات المُعتمدة سريريًا (مثل جهاز Enterra لعلاج شلل المعدة، ومحفزات VBLOC المبهمة لعلاج السمنة، وتحفيز InterStim العجزي لعلاج سلس البراز) تعمل بشكل أساسي في حلقة مفتوحة، وغالبًا ما تُنتج تأثيرات غير متسقة على إفراغ المعدة. والسبب هو أن مصدرًا واحدًا أو أكثر من مصادر التيار ذات المعلمات الثابتة لا يُحاكي التعقيد المكاني الزمني للتمعج الطبيعي.
- فسيولوجيا يجب "تقليدها". التمعج عبارة عن حلقة مغلقة: إشارات حسية (التمدد، درجة الحرارة، المحفزات الكيميائية) ← استجابات منعكسة في الضفيرة المعوية والعضلات الملساء. بالإضافة إلى نقل الطعام، تؤثر الحركة على إشارات الأمعاء والدماغ الواردة وهرمونات الشبع (GLP-1، الأنسولين، الغريلين)، مما يُشكل الشهية والشعور بالشبع. في حالة اختلال الحركة، تتعطل هذه الحلقات.
- الفجوة التكنولوجية. لإعادة إنتاج الموجات "الصحيحة"، يلزم تحفيز متعدد القنوات مباشرةً بالقرب من الضفيرة المعوية والطبقة العضلية. لكن الوصول إلى هناك يتطلب عادةً جراحةً باضعة؛ فالتقنيات التنظيرية المتقدمة (مثل NOTES) معقدة وقليلة الاستخدام. هناك حاجة إلى أدوات قليلة التوغل تسمح بوضع الأقطاب الكهربائية بدقة في الغشاء المخاطي السفلي، وتعمل في حلقة مغلقة من "الاستشعار ← التحفيز".
- ما يقدمه العمل الجديد. يصف الباحثون طرفًا عصبيًا اصطناعيًا متعدد القنوات مُركّبًا بالمنظار، مزودًا بتحفيز كهربائي وكيميائي، قادر على إطلاق موجات تمعجية منسقة عند إشارة مرور جرعة زائدة، مما لا يُعيد الحركة فحسب، بل يُعدّل أيضًا الاستجابة الأيضية (مما يجعلها أقرب إلى حالة "التغذية"). يُسدّ هذا ثغرات رئيسية: الوصول إلى الطبقة المطلوبة، والتنسيق الزماني المكاني، والعمل في حلقة مغلقة.
باختصار: هناك مجال سريري واسع - تثبيطات واسعة الانتشار وسوء المعالجة. المحفزات "المفتوحة" السابقة لا تحاكي وظائف الجسم الطبيعية. لذلك، من المنطقي محاولة تعليم الغرسة "التفكير مثل الجهاز الهضمي": استشعار اللقمة وتحفيز التمعج الفسيولوجي في المكان الذي تمر فيه الإشارة الطبيعية بالضبط - عند الضفيرة العضلية المعوية.
ابتكر فريق من معهد ماساتشوستس للتكنولوجيا وجامعة هارفارد وجامعة بريغهام غرسة مريئية/معدية مصغّرة تستشعر كمية الطعام في "حلقة مغلقة" وتُطلق موجات منسقة من التمعج. في الخنازير، لم يقتصر الجهاز على استعادة حركة المريء والمعدة فحسب، بل حفّز أيضًا تغيرات هرمونية مشابهة لحالة ما بعد الوجبة (التغذية). تُزرع الغرسة بالمنظار، دون جراحة في البطن. نُشرت الدراسة في مجلة نيتشر.
ماذا توصلوا إليه؟
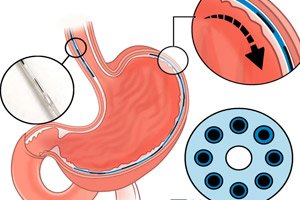
- الغرسة نفسها. دعامة عصبية ليفية رفيعة بقطر 1.25 مم تقريبًا، مزودة بسبعة أقطاب كهربائية كل سم واحد، وقناة دقيقة لتوصيل المواد موضعيًا (التحفيز الكهربائي والكيميائي). تسمح مرونتها وأبعادها بإدخالها عبر قناة أداة قياسية في منظار داخلي (2.8-3.2 مم).
- التركيب. طُوِّرت أداة تنظيرية: إبرة بسحب عكسي لـ"خطاف" نيتينول، وتشريح مائي، والحيلة الأساسية: البحث عن الغشاء المخاطي تحت المخاطي عن طريق معاوقة الأنسجة لتحديد موضعها بدقة فوق الطبقة العضلية مباشرةً، بالقرب من الضفيرة العضلية المعوية.
- حلقة مغلقة. يقرأ النظام إشارة الجرعة (مستشعرات تخطيط كهربية العضل/داخل التجويف) ويختار نمط تحفيز لتحفيز انقباضات متسلسلة مشابهة للتمعج الطبيعي. من الممكن الجمع بين المحفزات "المثيرة" و"المثبطة"، بالإضافة إلى إرخاء العضلات العاصرة موضعيًا بجرعات صغيرة من الأدوية.
ما تم عرضه على الحيوانات
- المريء: أنتجت الغرسة "موجات بلع" دون بلع فعلي، بما في ذلك الاسترخاء المتحكم به للعضلة العاصرة للمريء السفلية (عبر توصيل الجلوكاجون بشكل دقيق)، وموجات أمامية/رجعية قابلة للبرمجة - وهي في الأساس "عصا تحكم" تمعجية.
- المعدة. بعد 20 دقيقة من التحفيز، زاد تواتر التمعج حوالي الضعف مقارنةً بالمجموعة الضابطة (n≈4، p<0.05).
- وهم الشبع الأيضي. في حالات الصيام، أدى التحفيز لمدة 30 دقيقة (بالمريء أو المعدة) إلى تغيرات هرمونية: زيادة في GLP-1 والأنسولين، وانخفاض في جريلين (هرمون الشهية)؛ كما لوحظت زيادة في الجلوكاجون مع التحفيز المعدي. يشبه النمط الغذائي عمومًا حالة ما بعد الوجبة.
تفاصيل السلامة والهندسة
أظهرت اختبارات التوافق الحيوي المختبرية القصيرة (مستخلصات المواد) عدم وجود أي سمية؛ أما في الجسم الحي، فبعد 7 أيام من الزرع، كانت قابلية الجدار للتمدد طبيعية، ولم يحدث أي هجرة للجهاز أو تلف كبير في الأنسجة. (تتطلب المتانة والموثوقية إجراء اختبارات طويلة الأمد).
لماذا هذا ضروري؟
- خلل الحركة والحالات المقاومة للعلاج. تعذر الارتخاء المريئي، شلل المعدة، عسر البلع، اضطرابات ما بعد الجراحة - حيث غالبًا ما تُعطي الأدوية/العمليات الجراحية التقليدية تأثيرًا غير كامل. التحفيز الموضعي متعدد القنوات أقرب إلى وظائف الجسم الحقيقية من غرسات الحلقة المفتوحة أحادية القناة الحالية.
- الاضطرابات الأيضية. من خلال التحكم في مسارات الإشارات الواردة من الأمعاء إلى الدماغ، يُمكن للجهاز تعديل الشهية والتمثيل الغذائي، وهو أمرٌ مثيرٌ للاهتمام فيما يتعلق بالسمنة/داء السكري (فرضيةٌ حتى الآن، لا يوجد دليلٌ على ذلك لدى البشر).
القيود وما هو التالي
هذا عملٌ ما قبل سريري على الخنازير، في الوضع الحاد-شبه الحاد. وتجري دراساتٌ طويلة الأمد حول استقرار التلامس، وإمدادات الطاقة، وخطر التليف، وبروتوكولات تحفيز دقيقة، ثم تجارب سريرية مبكرة على مرضى يعانون من أشكال حادة من خلل الحركة. ولكن ثبت بالفعل أنه يمكن "تفعيل" التمعج عند الطلب، ويمكن تحويل الاستجابات الهرمونية نحو الشبع - كل ذلك من خلال الوصول بالمنظار.
