
تتم مراجعة جميع محتويات iLive طبياً أو التحقق من حقيقة الأمر لضمان أكبر قدر ممكن من الدقة الواقعية.
لدينا إرشادات صارمة من مصادرنا ونربط فقط بمواقع الوسائط ذات السمعة الطيبة ، ومؤسسات البحوث الأكاديمية ، وطبياً ، كلما أمكن ذلك استعراض الأقران الدراسات. لاحظ أن الأرقام الموجودة بين قوسين ([1] و [2] وما إلى ذلك) هي روابط قابلة للنقر على هذه الدراسات.
إذا كنت تشعر أن أيًا من المحتوى لدينا غير دقيق أو قديم. خلاف ذلك مشكوك فيه ، يرجى تحديده واضغط على Ctrl + Enter.
فيروس الحصبة (فيروس موربيلي)
خبير طبي في المقال
آخر مراجعة: 04.07.2025
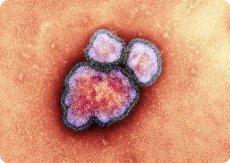
الحصبة (باللاتينية: morbilli) مرض فيروسي حاد يصيب الأطفال بشكل رئيسي، ويتميز بالتسمم العام والحمى ونزلات البرد في الأغشية المخاطية في الجهاز التنفسي والطفح الجلدي الحطاطي.
عُزل العامل المسبب للحصبة عام ١٩٥٤ على يد ج. إندرز وت. بيبلز. يشبه الفيروس من الناحية الشكلية الفيروسات الباراميكسوفيروسية الأخرى: يتراوح قطر الفيريون بين ١٥٠ و٢٥٠ نانومترًا، ويُمثل جينوم الفيروس جزيء RNA سلبي أحادي السلسلة غير مجزأ، يبلغ طوله ١٥٩٠٠ نوكليوتيد، مُدرجًا في غلاف نووي حلزوني. يحمل الجينوم ستة جينات مرتبة بالترتيب التالي: N، P، M، F، H، L. تُشفّر هذه الجينات البروتينات التالية: البروتين النووي (N)، والبروتين الفوسفوري (P)، والمصفوفة (M)، والبروتين الاندماجي (F)، والهيماغلوتينين (H)، والبوليميراز (L). ومن سمات الجينوم الفيروسي وجود منطقة كبيرة غير مُشفّرة في منطقته بين الجينات MF، تضم حوالي ١٠٠٠ نوكليوتيد. مثل الفيروسات المخاطية الأخرى، يمتلك فيروس الحصبة نشاطًا في تكتل الدم، وتحلل الدم، وتكوين الخلايا البلعمية، ولكنه يفتقر إلى النورامينيداز.
يختلف الهيماجلوتينين، والهيموليزين (F)، والنيوكليوبروتين (NP)، وبروتين المصفوفة في خصوصية المستضد ودرجة المناعة. يتميز الهيماجلوتينين بأعلى مناعة. تم الكشف عن العديد من المتغيرات المصلية لفيروس الحصبة البشري باستخدام الأجسام المضادة وحيدة النسيلة. كما أن له محددات مستضد مشتركة مع فيروسي حمى الكلاب وطاعون الماشية.
حيوانات المختبر ليست شديدة التأثر بفيروس الحصبة. يُسبب الفيروس مرضًا بأعراض سريرية مميزة لدى القرود فقط، وفي الظروف الطبيعية، يمكن أن تُصاب القرود بالعدوى من البشر.
يتكاثر فيروس الحصبة بشكل ضعيف في أجنة الدجاج. تُستخدم مزارع أولية مُعالجة بالتربسين من خلايا كلى القردة أو أجنة البشر لعزله. عند تكاثره، يُسبب الفيروس تأثيرًا خلويًا مميزًا (تكوين خلايا عملاقة متعددة النوى - البلاستيدات والخلايا المتزامنة - وشوائب حبيبية في السيتوبلازم والنواة). ومع ذلك، يُمكن أيضًا تكييف فيروس الحصبة مع مزارع خلايا كلى الكلاب والعجول، أو خلايا السلى البشرية، بالإضافة إلى سلالات مختلفة قابلة للزرع. يُمكن أن يكون للفيروس تأثير مُطفر على كروموسومات الخلايا.
الفيروس غير مستقر، ويفقد نشاطه بسرعة في البيئات الحمضية، ويقل نشاطه عند درجة حرارة 37 درجة مئوية، ويموت بعد 30 دقيقة عند درجة حرارة 56 درجة مئوية، ويسهل تدميره بمذيبات الدهون والمنظفات، وهو حساس جدًا لأشعة الشمس، ويموت بسرعة في البيئة الخارجية. كما أنه مقاوم لدرجات الحرارة المنخفضة (-70 درجة مئوية). يجب مراعاة هذه الظروف عند نقل وتخزين لقاح الحصبة الحي.
مسببات مرض الحصبة وأعراضه
تحدث العدوى عن طريق الرذاذ المحمول جوًا. يتكاثر الفيروس في الخلايا الظهارية للغشاء المخاطي للبلعوم الأنفي والقصبة الهوائية والشعب الهوائية. عند اختراقه للدم، فإنه يسبب تلفًا في الخلايا البطانية الوعائية، مما يؤدي إلى طفح جلدي. أكثر الأعراض المميزة هو تكوين بقع كوبليك-فيلاتوف على الغشاء المخاطي للخدين. فترة الحضانة حوالي 10 أيام. صورة المرض مميزة للغاية بحيث يسهل تشخيصها سريريًا. في الفترة الباكرة - أعراض التهابات الجهاز التنفسي الحادة (التهاب الأنف، التهاب البلعوم، التهاب الملتحمة). ظهور بقع كوبليك-فيلاتوف له أهمية تشخيصية تفاضلية. يظهر الطفح الجلدي الحطاطي عادةً في اليوم الرابع بعد ارتفاع درجة الحرارة، أولاً على الرأس (الجبهة، خلف الأذنين)، ثم ينتشر في جميع أنحاء الجسم. تعود درجة حرارة الجسم إلى طبيعتها بحلول اليوم السابع أو الثامن.
المضاعفات الأكثر شيوعًا هي الالتهاب الرئوي، وفي المراحل المبكرة من المرض - وذمة الحنجرة، والخانوق. نادرًا ما تحدث الحصبة بشكل غير عادي وشديد - على شكل التهاب دماغي حاد ناتج عن الحصبة، وهو أكثر شيوعًا لدى الأطفال الذين تتراوح أعمارهم بين 8 و10 سنوات. أما الأطفال الذين تلقوا الغلوبولين المناعي للحصبة لأغراض وقائية، فيظهر المرض بشكل خفيف (حصبة مخففة). تكون المناعة بعد الإصابة قوية وتستمر مدى الحياة، بفضل الأجسام المضادة المُحيِّدة للفيروس، والخلايا الليمفاوية التائية السامة، وخلايا الذاكرة المناعية.
التهاب الدماغ الشامل المصلب تحت الحاد
لا يُسبب فيروس الحصبة عدوى حادة مُنتجة فحسب، وهي الحصبة، بل يُسبب أيضًا، في حالات نادرة جدًا، عدوى بطيئة شديدة - التهاب الدماغ الشامل المصلب تحت الحاد (SSPE). وُصف هذا المرض لأول مرة عام ١٩٣٣ من قِبل ج. داوسون، وهو مرض مُتفاقم يُصيب الجهاز العصبي المركزي لدى الأطفال والمراهقين. يُصبح الأطفال المرضى سريعي الانفعال، وسريعي البكاء، ويضعف كلامهم وبصرهم، ويتوقفون عن تمييز الأشياء المحيطة بهم؛ وسرعان ما يُعاني المرضى من انخفاض في الذكاء، وغيبوبة، ثم الوفاة.
ظل سبب هذا المرض غامضًا لفترة طويلة. في ستينيات القرن الماضي، عُثر على أجسام مضادة للحصبة بتركيزات عالية (تصل إلى 1:16,000) لدى الأطفال المرضى، كما عُثر في خلايا الدماغ على شوائب مميزة للحصبة تحتوي على كبسولات نووية مشابهة لفيروسات الباراميكسو. وأخيرًا، عُزلت سلالات مشابهة لفيروس الحصبة من أنسجة المخ والعقد اللمفاوية لدى المتوفين.
يتطور المرض عند دخول فيروس الحصبة إلى خلايا الجهاز العصبي المركزي. يتعطل تكاثر الفيروس في هذه الخلايا في مرحلة التخلق، على ما يبدو بسبب غياب بروتين M (لا يتم الكشف عن الأجسام المضادة لمستضد M لدى هؤلاء المرضى). ونتيجة لذلك، يتراكم عدد كبير من الفيروسات المعيبة التي تفتقر إلى القفيصة الفائقة وبروتين M في الخلايا. قد تكون الآليات الجزيئية لتعطيل تخليق البروتين الفيروسي مختلفة. يرتبط أحدها بوجود تدرج في مستوى النسخ، والذي يتجلى في حقيقة أن الجينات البعيدة عن الطرف 3' من الحمض النووي الريبي الجينومي يتم نسخها بدرجة أقل من الجينات الموجودة بالقرب منها. إذا كانت مستويات نسخ الجينات القريبة والبعيدة عن الطرف 3' في عدوى الحصبة الحادة تختلف بما لا يزيد عن 5 مرات، فإن هذه الاختلافات تصل في PSPE إلى مستوى 200 ضعف. يؤدي هذا إلى انخفاض في تخليق البروتينات M وF وH إلى ما دون المستوى اللازم لتكوين الفيريون وتبرعمه، أي إلى تكوين وتراكم الجسيمات المتداخلة المعيبة (DIP). ربما لأن آلية تطور SSPE تعتمد على اضطرابات ليس فقط في المناعة، بل أيضًا في بعض الآليات الجينية.
تشخيص الحصبة
يُجرى تشخيص الحصبة مختبريًا عند الضرورة. ويُقترح نظام اختبار لتحديد جينوم فيروس الحصبة يعتمد على نسخة أحادية الأنبوب من تفاعل النسخ العكسي مع تفاعل البوليميراز المتسلسل (PCR) (باستخدام بوليميراز مُعدّل). لعزل الفيروس، تُصاب مزارع الخلايا بمادة الاختبار (مخاط البلعوم الأنفي، الدم) قبل يوم واحد من ظهور الطفح الجلدي. يُحدد الفيروس باستخدام RIF وRTGA وRN في مزارع الخلايا. تُستخدم RTGA وIFM وRSC لمراقبة حالة المناعة.
الوقاية المحددة من الحصبة
الوسيلة الجذرية الوحيدة لمكافحة الحصبة هي التطعيم. ولهذا الغرض، تُستخدم لقاحات حية عالية الفعالية من سلالات حصبة مُضعَّفة (من سلالة L-16 وسلالة M-5). ومن المتوقع القضاء على الحصبة في المنطقة الأوروبية بحلول عام 2007، وبحلول عام 2010، ينبغي اعتماد القضاء عليها في جميع دول العالم.
اقرأ أيضًا: التطعيم ضد الحصبة والنكاف والحصبة الألمانية
لتحقيق ذلك، من الضروري تطعيم 98-100% من الأطفال حديثي الولادة الذين تتراوح أعمارهم بين 9 و12 شهرًا. بالإضافة إلى ذلك، من الضروري إعادة تطعيم جميع الأطفال الذين تتراوح أعمارهم بين 9 و10 أشهر و14-16 عامًا كل 5-7 سنوات لتقليل عدد الأشخاص المعرضين للإصابة بالحصبة.


 [
[