
تتم مراجعة جميع محتويات iLive طبياً أو التحقق من حقيقة الأمر لضمان أكبر قدر ممكن من الدقة الواقعية.
لدينا إرشادات صارمة من مصادرنا ونربط فقط بمواقع الوسائط ذات السمعة الطيبة ، ومؤسسات البحوث الأكاديمية ، وطبياً ، كلما أمكن ذلك استعراض الأقران الدراسات. لاحظ أن الأرقام الموجودة بين قوسين ([1] و [2] وما إلى ذلك) هي روابط قابلة للنقر على هذه الدراسات.
إذا كنت تشعر أن أيًا من المحتوى لدينا غير دقيق أو قديم. خلاف ذلك مشكوك فيه ، يرجى تحديده واضغط على Ctrl + Enter.
عدم تنسج النخاع العظمي
خبير طبي في المقال
آخر مراجعة: 04.07.2025
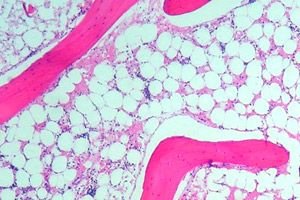
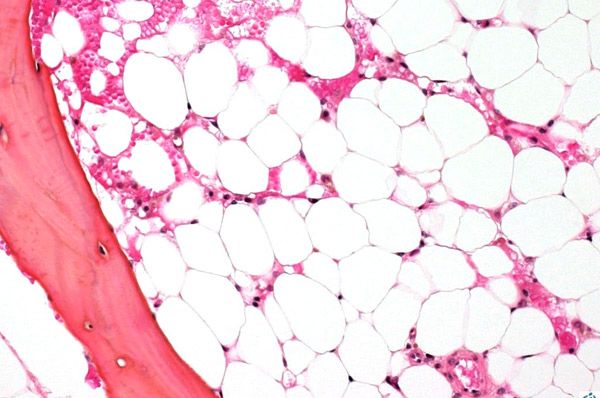
خلل تنسج نخاع العظم (أو خلل تكوين الدم) هو متلازمة قصور نخاع العظم، تشمل مجموعة من الاضطرابات التي تُضعف وظيفة تكوين الدم التي يؤديها نخاع العظم بشكل حاد. وينتج عن هذا الاضطراب قلة الكريات الشاملة (نقص في جميع خلايا الدم: الكريات البيضاء، وكريات الدم الحمراء، والصفائح الدموية). ويُعد قلة الكريات الشاملة الشديدة حالةً مهددةً للحياة.
الأسباب عدم تنسج النخاع العظمي
تشمل أسباب عدم تنسج نخاع العظم ما يلي:
- العلاج الكيميائي والعلاج الإشعاعي.
- اضطرابات المناعة الذاتية.
- ظروف العمل الضارة بالبيئة.
- عدوى فيروسية مختلفة.
- التلامس مع مبيدات الأعشاب والمبيدات الحشرية.
- بعض الأدوية، مثل تلك المستخدمة لعلاج التهاب المفاصل الروماتويدي أو المضادات الحيوية.
- بيلة الهيموجلوبين الليلية.
- فقر الدم الانحلالي.
- أمراض النسيج الضام.
- الحمل - يتعرض نخاع العظم للتلف بسبب رد فعل منحرف للجهاز المناعي.
عوامل الخطر
ومن بين عوامل الخطر المؤدية إلى عدم تنسج نخاع العظم تلك الموضحة أدناه.
- المركبات الكيميائية: مُثبِّطات الخلايا - تُساعد على إيقاف انقسام الخلايا، وتُستخدم عادةً لعلاج الأورام. قد تُؤدِّي جرعة مُعيَّنة من هذه الأدوية إلى إتلاف نخاع العظم، مما يُعطِّل تكوين خلايا الدم؛ مُثبِّطات المناعة - تُثبِّط جهاز المناعة في الجسم، وتُستخدَم عند حدوث نشاط مُفرط للجهاز المناعي، مما يُؤدِّي إلى إتلاف أنسجته السليمة. عند التوقف عن تناولها، غالبًا ما تُستعاد عملية تكوين الدم.
- المواد التي تؤثر على الجسم إذا كان لدى المريض حساسية مفرطة تجاهها. وتشمل هذه المواد المضادات الحيوية (الأدوية المضادة للبكتيريا)، والبنزين، والزئبق، والأصباغ المختلفة، والكلورامفينيكول، ومستحضرات الذهب. يمكن أن تسبب هذه المواد تلفًا عكسيًا وغير عكسي لوظيفة نخاع العظم. ويمكن أن تدخل الجسم عبر الجلد، أو استنشاق الهباء الجوي، أو عن طريق الفم مع الماء والطعام.
- التعرض للجزيئات الأيونية (الإشعاع) - على سبيل المثال، إذا تم انتهاك لوائح السلامة في محطات الطاقة النووية أو في المؤسسات الطبية حيث يتم علاج الأورام باستخدام العلاج الإشعاعي؛
- العدوى الفيروسية - مثل الأنفلونزا، وفيروس التهاب الكبد، وما إلى ذلك.
طريقة تطور المرض
لم تُدرس بعدُ آلية تطور خلل تنسج نخاع العظم دراسةً كاملة. ويجري حاليًا دراسة عدة آليات مختلفة لتطوره:
- يتأثر نخاع العظم من خلال الخلايا الجذعية متعددة القدرات؛
- يتم قمع عملية تكوين الدم بسبب تأثير الآليات المناعية الخلطية أو الخلوية؛
- تبدأ مكونات البيئة المحيطة بالعمل بشكل غير صحيح؛
- تطور نقص العوامل التي تعزز عملية تكوين الدم.
- الطفرات في الجينات التي تسبب متلازمات فشل نخاع العظم الوراثي.
في هذا المرض لا ينخفض محتوى المكونات (فيتامين ب12، والحديد، والبروتوبورفيرين)، التي تشارك بشكل مباشر في تكون الدم، ولكن في نفس الوقت لا تستطيع الأنسجة المكونة للدم استخدامها.
الأعراض عدم تنسج النخاع العظمي
يتجلى خلل تنسج نخاع العظم اعتمادًا على العنصر الخلوي في الدم الذي تأثر:
- إذا كان هناك انخفاض في مستوى خلايا الدم الحمراء، وضيق في التنفس، وضعف عام وأعراض أخرى لفقر الدم تظهر؛
- إذا انخفض مستوى خلايا الدم البيضاء يحدث الحمى وتزداد قابلية الجسم للإصابة بالعدوى؛
- إذا انخفض مستوى الصفائح الدموية، يكون هناك ميل لتطوير متلازمة النزف، والنزيف، والاحمرار.
في حالة خلل تنسج خلايا الدم الحمراء الجزئي في نخاع العظم، يتم ملاحظة انخفاض حاد في إنتاج خلايا الدم الحمراء، وقلة الشبكية العميقة، وفقر الدم الكروماتوجرافي المعزول.
هناك أشكال خلقية ومكتسبة لهذا المرض. يتجلى النوع الثاني في شكل سُلال كريات الدم الحمراء الأولي المكتسب، بالإضافة إلى متلازمة تحدث مع أمراض أخرى (مثل سرطان الرئة، والتهاب الكبد، وسرطان الدم، وداء وحيدات النوى المعدي، أو الالتهاب الرئوي، بالإضافة إلى فقر الدم المنجلي، والنكاف، والتهاب القولون التقرحي، إلخ).
المضاعفات والنتائج
تشمل مضاعفات عدم تنسج نخاع العظم ما يلي:
- غيبوبة فقر الدم، التي يُفقد فيها المريض الوعي، ويدخل في حالة غيبوبة. لا يُلاحظ أي رد فعل تجاه أي مُحفزات خارجية، إذ لا يصل الأكسجين إلى الدماغ بالكميات المطلوبة، وذلك بسبب انخفاض مستوى خلايا الدم الحمراء في الدم بسرعة وبشكل ملحوظ.
- تبدأ حالات نزيف مختلفة (مضاعفات نزفية). أسوأ خيار في هذه الحالة هو السكتة الدماغية النزفية (حيث يمتلئ جزء من الدماغ بالدم، ويموت نتيجة لذلك).
- العدوى - تسبب الكائنات الحية الدقيقة (مختلف الفطريات والبكتيريا أو الفيروسات) أمراضًا معدية؛
- ضعف الحالة الوظيفية لبعض الأعضاء الداخلية (مثل الكلى أو القلب)، وخاصة مع الأمراض المزمنة المصاحبة.
التشخيص عدم تنسج النخاع العظمي
عند تشخيص مرض عدم تنسج نخاع العظم، يتم دراسة التاريخ الطبي للمريض وشكواه: منذ متى ظهرت أعراض المرض، وما الذي يربطه المريض بمظهرها.
بعد ذلك يتم توضيح تاريخ حياة المريض:
- وجود أمراض مزمنة مصاحبة لدى المريض.
- وجود أمراض وراثية.
- هل لدى المريض أي عادات سيئة؟
- يتم توضيح ما إذا كان قد تم تناول أي أدوية مؤخرًا لفترة طويلة.
- وجود أورام لدى المريض.
- هل كان هناك اتصال مع عناصر سامة مختلفة؟
- هل تعرض المريض للإشعاع أو عوامل إشعاعية أخرى؟
بعد ذلك، يُجرى فحص بدني. يُحدَّد لون الجلد (في حال وجود شحوب في نخاع العظم)، ويُحدَّد معدل النبض (غالبًا ما يكون سريعًا)، ومؤشرات ضغط الدم (منخفض). تُفحَص الأغشية المخاطية والجلد بحثًا عن أي نزيف أو حويصلات صديدية، وما إلى ذلك.
الاختبارات
خلال عملية تشخيص المرض، يتم إجراء بعض الفحوصات المخبرية أيضًا.
يُجرى فحص دم - إذا كان المريض يُعاني من خلل في نخاع العظم، فسيتم الكشف عن انخفاض في مستوى الهيموغلوبين وعدد خلايا الدم الحمراء. يبقى مؤشر لون الدم طبيعيًا. ينخفض عدد الصفائح الدموية مع الكريات البيضاء، بالإضافة إلى اختلال النسبة الصحيحة للكريات البيضاء بسبب انخفاض محتوى الخلايا المحببة.
يتم إجراء اختبار البول أيضًا لتحديد وجود خلايا الدم الحمراء في البول - وهذا دليل على وجود متلازمة النزف، أو وجود كريات الدم البيضاء والكائنات الحية الدقيقة، وهو أحد أعراض تطور المضاعفات المعدية في الجسم.
يُجرى أيضًا فحص دم كيميائي حيوي. يُحدد هذا الفحص مستويات الجلوكوز، والكوليسترول، وحمض اليوريك (لتحديد أي تلف مصاحب في أي عضو)، والكرياتينين، والشوارد (الصوديوم، والبوتاسيوم، والكالسيوم).
 [ 38 ]، [ 39 ]، [ 40 ]، [ 41 ]، [ 42 ]، [ 43 ]، [ 44 ]
[ 38 ]، [ 39 ]، [ 40 ]، [ 41 ]، [ 42 ]، [ 43 ]، [ 44 ]
التشخيص الآلي
أثناء التشخيص الآلي يتم تنفيذ الإجراءات التالية.
لفحص نخاع العظم، يُجرى ثقب (يُستخرج خلاله المحتوى الداخلي) لعظمة، عادةً عظمة القص أو الورك. وبمساعدة الفحص المجهري، يُحدد استبدال الأنسجة المكونة للدم بندبة أو دهون.
خزعة بالمثقب، والتي تُفحص نخاع العظم وعلاقته بالأنسجة المجاورة. خلال هذا الإجراء، يُستخدم جهاز خاص يُسمى المثقب، وبمساعدته، يُؤخذ عمود من نخاع العظم من عظمة الحرقفة مع السمحاق والعظم.
تخطيط كهربية القلب، الذي يسمح بتحديد المشاكل المتعلقة بتغذية عضلة القلب وإيقاع القلب.
ما هي الاختبارات المطلوبة؟
تشخيص متباين
يتم إجراء التشخيص التفريقي مع الأمراض التالية:
- بيلة الهيموغلوبين الانتيابية الليلية ؛
- فقر الدم الناقص التنسج (وكذلك نقص الكريات الحمراء العابر عند الأطفال)؛
- فرط نشاط الطحال ؛
- متلازمة خلل التنسج النقوي ؛
- سرطان الدم الحاد والخلايا المشعرة ؛
- إس كي في ؛
- متلازمة DIC ؛
- فقر الدم الذي يتطور نتيجة لقصور الغدة النخامية أو قصور الغدة الدرقية أو أمراض الكبد.
من الاتصال؟
علاج او معاملة عدم تنسج النخاع العظمي
يكاد يكون من المستحيل القضاء على المرض باستخدام العلاج المُسبب (بالتأثير على سببه). قد يُساعد إزالة العامل المُسبب (مثل إيقاف الدواء، أو مغادرة منطقة الإشعاع، إلخ)، ولكن في هذه الحالة، ينخفض معدل موت نخاع العظم فقط، ولكن لا يُمكن استعادة تكوين الدم المستقر بهذه الطريقة.
يُستخدم العلاج المثبط للمناعة في حال تعذر إجراء عملية الزرع (في حال عدم وجود متبرع مناسب للمريض). في هذه الحالة، تُستخدم أدوية من مجموعة السيكلوسبورين أ أو مجموعة الجلوبيولين المضاد للخلايا الليمفاوية. وأحيانًا يُستخدمان معًا.
استخدام GM-CSF (أدوية تُحفّز إنتاج خلايا الدم البيضاء). يُستخدم هذا العلاج إذا انخفض عدد خلايا الدم البيضاء إلى أقل من ٢×١٠٩ جم/لتر. كما يُمكن استخدام أدوية الكورتيكوستيرويد في هذه الحالة.
يتم استخدام المنشطات الابتنائية، والتي تحفز تكوين البروتين.
يتم استخدام الطرق التالية في علاج خلل تنسج نخاع العظم:
- نقل عناصر الدم.
تُجرى عمليات نقل الدم باستخدام خلايا دم حمراء مغسولة (خلايا دم حمراء من المتبرع خالية من البروتينات). تُقلل هذه الطريقة من شدة وعدد ردود الفعل السلبية الناتجة عن عملية نقل الدم. لا تُجرى عمليات نقل الدم هذه إلا في حال وجود خطر على حياة المريض. وتشمل الحالات التالية:
- يدخل المريض في غيبوبة فقر الدم؛
- فقر الدم الشديد (في هذه الحالة ينخفض مستوى الهيموجلوبين إلى أقل من 70 جم/ل).
يتم إجراء نقل الصفائح الدموية من المتبرع إذا كان المريض يعاني من نزيف وانخفاض واضح في عدد الصفائح الدموية.
يتم إجراء العلاج المرقئ اعتمادًا على المنطقة التي بدأ فيها النزيف.
عند حدوث مضاعفات معدية يتم اللجوء إلى طرق العلاج التالية:
- العلاج بالمضادات الحيوية. يُجرى هذا العلاج بعد أخذ مسحات من البلعوم الأنفي، بالإضافة إلى مزارع للبول والدم، لتحديد نوع الكائن الدقيق المسبب للعدوى، وقياس حساسيته للمضادات الحيوية.
- العلاج المضاد للفطريات الجهازي إلزامي؛
- علاج موضعي بمطهرات للمناطق التي قد تصبح نقاط دخول للعدوى (وهي الأماكن التي تدخل منها البكتيريا أو الفطريات أو الفيروسات إلى الجسم). تتضمن هذه الإجراءات عادةً المضمضة باستخدام أدوية مختلفة بالتناوب.
الأدوية
في حالة عدم تنسج نخاع العظم، يكون العلاج الدوائي إلزاميًا. الأدوية الأكثر شيوعًا هي تلك التي تنتمي إلى ثلاث مجموعات دوائية: مُثبِّطات الخلايا (6-ميركابتوبيوريل، سيكلوفوسفاميد، ميثوتريكسات، سيكلوسبورين أ، وإيموران)، ومثبطات المناعة (ديكساميثازون، وميثيل بريدنيزولون)، والمضادات الحيوية (ماكروليدات، سيفالوسبورينات، كلوروكينولون، وأزاليدات). في بعض الأحيان، يمكن استخدام أدوية لعلاج اضطرابات البكتيريا المعوية ومشاكل ضغط الدم، وأدوية الإنزيم، وما إلى ذلك.
يُوصف ميثيل بريدنيزولون فمويًا. في حالة زراعة الأعضاء، لا تتجاوز الجرعة 0.007 غ/يوم.
الأعراض الجانبية للدواء: قد يتم احتباس الماء والصوديوم في الجسم، ارتفاع ضغط الدم، قد يحدث فقدان البوتاسيوم، هشاشة العظام، ضعف العضلات، التهاب المعدة الناجم عن الدواء، قد تقل مقاومة العدوى المختلفة، قمع نشاط الغدة الكظرية، بعض الاضطرابات النفسية، مشاكل في الدورة الشهرية.
يُمنع استعمال الدواء في حالات ارتفاع ضغط الدم الشديد، وفشل الدورة الدموية في المرحلة الثالثة، وكذلك الحمل والتهاب الشغاف الحاد، وكذلك التهاب الكلية، والذهان المتنوع، وهشاشة العظام، وقرحة الاثني عشر أو المعدة؛ بعد العملية الجراحية الحديثة؛ في المرحلة النشطة من مرض السل، والزهري؛ في كبار السن، وكذلك في الأطفال دون سن 12 عامًا.
يُوصف ميثيل بريدنيزولون بحذر في حالة الإصابة بداء السكري، فقط في حال وجود دواعي استعمال مطلقة، أو لعلاج المرضى الذين يعانون من مقاومة الأنسولين، والذين لديهم مستويات عالية من الأجسام المضادة للأنسولين. في حالات السل أو الأمراض المُعدية، لا يُستخدم الدواء إلا مع المضادات الحيوية أو أدوية علاج السل.
إيموران - يُسمح في اليوم الأول باستخدام جرعة لا تتجاوز 5 ملغ لكل كيلوغرام من وزن الجسم يوميًا (يجب تناولها على جرعتين أو ثلاث جرعات)، إلا أن الجرعة تعتمد عمومًا على نظام تثبيط المناعة. تتراوح جرعة الصيانة بين 1 و4 ملغ لكل كيلوغرام من الوزن يوميًا. وتُحدد الجرعة بناءً على قدرة جسم المريض على تحمل الدواء وحالته السريرية. تشير الدراسات إلى أن العلاج بإيموران يجب أن يستمر لفترة طويلة، حتى بجرعات صغيرة.
قد تُسبب الجرعة الزائدة تقرحات في الحلق، ونزيفًا وكدمات، والتهابات. هذه الأعراض أكثر شيوعًا في حالات الجرعة الزائدة المزمنة.
الآثار الجانبية - بعد زراعة نخاع العظم، غالبًا ما يُصاب المرضى الذين يُعالَجون بالآزاثيوبرين مع مثبطات مناعة أخرى بعدوى بكتيرية أو فطرية أو فيروسية. تشمل الآثار الجانبية الأخرى عدم انتظام ضربات القلب، وأعراض التهاب السحايا، والصداع، وإصابات الشفتين والفم، والتنمل، وغيرها.
يُعطى السيكلوسبورين أ وريديًا - تُقسّم الجرعة اليومية إلى جرعتين وتُعطى قبل العملية بفترة تتراوح بين ساعتين وست ساعات. الجرعة اليومية الأولية كافية، وتتراوح بين 3 و5 ملغم/كغم. يُعدّ الإعطاء الوريدي الأمثل لعلاج المرضى الذين خضعوا لزراعة نخاع العظم. قبل عملية الزرع (4-12 ساعة قبل العملية)، يُعطى المريض جرعة تتراوح بين 10 و15 ملغم/كغم عن طريق الفم، ثم تُعطى الجرعة اليومية نفسها لمدة أسبوع أو أسبوعين. بعد ذلك، تُخفّض الجرعة إلى جرعة الصيانة المعتادة (حوالي 2-6 ملغم/كغم).
تشمل أعراض الجرعة الزائدة النعاس والقيء الشديد وتسارع القلب والصداع وتطور الفشل الكلوي الحاد.
عند تناول السيكلوسبورين، يجب اتباع الاحتياطات التالية. يجب أن يُدار العلاج في المستشفى من قِبل أطباء ذوي خبرة واسعة في علاج المرضى الذين يستخدمون مثبطات المناعة. تجدر الإشارة إلى أن تناول السيكلوسبورين يزيد من احتمالية الإصابة بأورام تكاثرية لمفاوية خبيثة. لذلك، من الضروري تحديد ما إذا كانت الفائدة العلاجية تبرر جميع المخاطر المصاحبة قبل البدء بتناوله. يُسمح باستخدام الدواء أثناء الحمل فقط في حالات الضرورة القصوى. ونظرًا لخطر حدوث تفاعلات تأقية نتيجة الإعطاء الوريدي، يجب تناول مضادات الهيستامين للوقاية، ويجب تحويل المريضة إلى تناول الدواء عن طريق الفم في أسرع وقت ممكن.
الفيتامينات
في حال معاناة المريض من نزيف، يُنصح، بالإضافة إلى العلاج بالدم، بتناول محلول كلوريد الكالسيوم بتركيز 10% (عن طريق الفم)، بالإضافة إلى فيتامين ك (15-20 ملغ يوميًا). كما يُوصف حمض الأسكوربيك بكميات كبيرة (0.5-1 غ/يوم) وفيتامين ب (بجرعة 0.15-0.3 غ/يوم). ويُنصح بتناول حمض الفوليك بجرعات كبيرة (بحد أقصى 200 ملغ/يوم)، بالإضافة إلى فيتامين ب6، ويفضل أن يكون ذلك على شكل حقن (50 ملغ من البيريدوكسين يوميًا).
العلاج الطبيعي
لتنشيط نخاع العظم، يُستخدم العلاج الطبيعي - وهو عبارة عن ضخّ عظام أنبوبية في منطقة قصبة الساق أو القص. يُجرى هذا الإجراء يوميًا لمدة 20 دقيقة. تجدر الإشارة إلى أن هذا الخيار ممكن فقط في حال عدم وجود نزيف حاد.
العلاج الجراحي
تُجرى عملية زراعة نخاع العظم في حالات عدم التنسج الشديد. تزداد فعالية هذه العملية إذا كان المريض صغير السن وتلقى عددًا قليلًا من عمليات نقل الدم من متبرعين (لا يزيد عن ١٠ عمليات).
يتضمن هذا العلاج استخراج نخاع العظم من المتبرع ثم زراعته في المتلقي. قبل إدخال معلق الخلايا الجذعية، يُعالَج بمضادات تثبيط الخلايا.
بعد عملية الزرع، سيخضع المريض لدورة طويلة من العلاج المثبط للمناعة، وهو أمر ضروري لمنع رفض الجسم للزرع، وكذلك لمنع ردود الفعل المناعية السلبية الأخرى.
الوقاية
تتمثل الإجراءات الوقائية الأساسية المتعلقة بعدم تنسج نخاع العظم فيما يلي: الوقاية من تأثير العوامل الخارجية السلبية على الجسم. ولتحقيق ذلك، يجب مراعاة احتياطات السلامة عند التعامل مع الأصباغ أو المواد التي قد تكون مصادر للإشعاع المؤين، وكذلك مراقبة عملية استخدام الأدوية.
الوقاية الثانوية، والتي تعد ضرورية لمنع التدهور المحتمل لحالة الشخص المصاب بمرض متطور بالفعل أو لمنع الانتكاس، تتكون من التدابير التالية:
- مراقبة المرضى الخارجيين. يجب أن تستمر المراقبة حتى لو أظهر المريض علامات تعافي؛
- العلاج الدوائي الداعم طويل الأمد.
توقعات
عادةً ما يكون تشخيص خلل تنسج نخاع العظم غير مواتٍ - إذا لم يتم إجراء العلاج في الوقت المناسب، يموت المريض في 90٪ من الحالات.
بفضل زراعة نخاع العظم من متبرع، يمكن لـ 9 من كل 10 مرضى أن يعيشوا أكثر من 5 سنوات. لذلك، تُعتبر هذه الطريقة العلاج الأكثر فعالية.
أحيانًا لا يكون إجراء عملية زرع ممكنًا، لكن العلاج الدوائي الحديث يُعطي نتائج إيجابية. بفضله، يعيش حوالي نصف المرضى لأكثر من خمس سنوات. ولكن في معظم الحالات، يبقى المرضى الذين أصيبوا بالمرض قبل سن الأربعين على قيد الحياة.
قائمة الكتب والدراسات الموثوقة المتعلقة بدراسة عدم تنسج نخاع العظم
- كتاب: "فقر الدم اللاتنسجي: الفيزيولوجيا المرضية والعلاج" المؤلف: هوبرت شريزينماير وأندريا باسيجالوبو السنة: ٢٠٠٩
- كتاب: "فقر الدم اللاتنسجي ومتلازمات فشل نخاع العظم الأخرى" تأليف: نيل س. يونغ وكولين ج. ستيوارد، سنة النشر: ٢٠١٨
- دراسة: "تشخيص وعلاج فقر الدم اللاتنسجي المكتسب لدى الأطفال" المؤلفان: مونيكا بيسلر وبلانش ب. ألتر، سنة النشر: ٢٠١٦
- دراسة: "فقر الدم اللاتنسجي: التسبب في المرض، التشخيص، والعلاج" للمؤلف: ياروسلاف ب. ماسيجوسكي ونيل س. يونغ، عام ٢٠١٨
- كتاب: "فقر الدم اللاتنسجي" المؤلف: جون دبليو. آدمسون السنة: ٢٠٠٩

