
تتم مراجعة جميع محتويات iLive طبياً أو التحقق من حقيقة الأمر لضمان أكبر قدر ممكن من الدقة الواقعية.
لدينا إرشادات صارمة من مصادرنا ونربط فقط بمواقع الوسائط ذات السمعة الطيبة ، ومؤسسات البحوث الأكاديمية ، وطبياً ، كلما أمكن ذلك استعراض الأقران الدراسات. لاحظ أن الأرقام الموجودة بين قوسين ([1] و [2] وما إلى ذلك) هي روابط قابلة للنقر على هذه الدراسات.
إذا كنت تشعر أن أيًا من المحتوى لدينا غير دقيق أو قديم. خلاف ذلك مشكوك فيه ، يرجى تحديده واضغط على Ctrl + Enter.
تقوم الخلايا السرطانية بتنشيط إنتاج الطاقة على الفور عندما يتم ضغط الحمض النووي وتلفه
آخر مراجعة: 03.08.2025
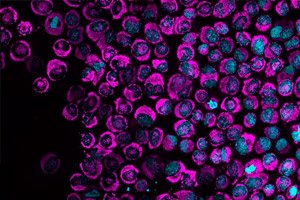
وفقًا لدراسة نُشرت في مجلة Nature Communications ، تُنشّط الخلايا السرطانية استجابةً غنيةً بالطاقة فورًا عند الضغط عليها. تُعد هذه الدفعة من الطاقة أول دليل مُوثّق على آلية حماية تُساعد الخلايا على إصلاح الحمض النووي التالف والصمود في ظلّ الظروف القاسية لجسم الإنسان.
تساعد هذه النتائج في تفسير كيفية بقاء الخلايا السرطانية على قيد الحياة في بيئات ميكانيكية معقدة، كالزحف عبر بيئات الورم الدقيقة، واختراق الأوعية الدموية المسامية، أو التغلب على الصدمات في مجرى الدم. قد يؤدي اكتشاف هذه الآلية إلى استراتيجيات جديدة لتثبيت الخلايا السرطانية قبل انتشارها.
حقق باحثون في مركز تنظيم الجينوم (CRG) في برشلونة هذا الاكتشاف باستخدام مجهر متخصص قادر على ضغط الخلايا الحية إلى عرض ثلاثة ميكرونات فقط، أي أصغر بثلاثين مرة تقريبًا من قطر شعرة الإنسان. ولاحظوا أنه في غضون ثوانٍ من الضغط، تندفع الميتوكوندريا في خلايا هيلا إلى سطح النواة وتبدأ بضخ كميات إضافية من ATP، وهو مصدر الطاقة الجزيئية للخلايا.
هذا يدفعنا إلى إعادة النظر في دور الميتوكوندريا في جسم الإنسان. فهي ليست مجرد بطاريات ثابتة تُغذي الخلايا، بل هي "منقذات" بارعة يُمكن الاستعانة بها في حالات الطوارئ عندما تُدفع الخلية إلى أقصى طاقتها، كما تقول الدكتورة سارة سديلشي، المؤلفة المشاركة في الدراسة.
شكلت الميتوكوندريا توهجًا كثيفًا حول النواة لدرجة أن النواة انضغطت إلى الداخل. لوحظت هذه الظاهرة في 84% من خلايا سرطان هيلا المضغوطة، مقارنةً بانعدامها تقريبًا في الخلايا العائمة غير المضغوطة. أطلق الباحثون على هذه البُنى اسم NAM، وهو اختصار لـ "الميتوكوندريا المرتبطة بالنواة".
لمعرفة ما تفعله الخلايا العصبية الاصطناعية (NAMs)، استخدم الباحثون مستشعرًا فلوريًا يضيء عند دخول ATP إلى النواة. ازدادت الإشارة بنحو 60% بعد ثلاث ثوانٍ فقط من ضغط الخلايا.
يقول الدكتور فابيو بيزانو، المؤلف المشارك الأول للدراسة: "هذه علامة واضحة على أن الخلايا تتكيف مع الضغوط وتعيد تشكيل عملية التمثيل الغذائي الخاصة بها".
أظهرت تجارب أخرى أهمية هذه الزيادة في الطاقة. يُجهد الضغط الميكانيكي الحمض النووي، مُكسرًا خيوطه ومُتشابكًا في الجينوم. تحتاج الخلايا إلى مُعقدات إصلاح تعتمد على ATP لإضعاف بنية الحمض النووي ومعالجة الضرر. أصلحت الخلايا المضغوطة التي تلقت ATP إضافيًا حمضها النووي في غضون ساعات، بينما توقفت الخلايا التي لم تتلقى ATP الإضافي عن الانقسام بشكل طبيعي.
لتأكيد أهمية هذه الآلية في المرض، فحص الباحثون أيضًا خزعات من أورام الثدي لدى 17 مريضًا. ولوحظت هالات NAM في 5.4% من النوى عند الهامش الغازي للورم، مقارنةً بـ 1.8% في النواة الكثيفة - وهو فرق ثلاثة أضعاف.
يقول الدكتور ريتوبراتا (ريتو) جوس، المؤلف المشارك الأول في الدراسة: "إن حقيقة أننا وجدنا هذا التوقيع في أنسجة المريض أكدت أهميته خارج المختبر".
تمكن الباحثون أيضًا من دراسة الآليات الخلوية التي تُمكّن من "تدفق" الميتوكوندريا. تُشكّل خيوط الأكتين - وهي نفس الخيوط البروتينية التي تسمح للعضلات بالانقباض - حلقة حول النواة، وتسحب الشبكة الإندوبلازمية هذا "الفخ" الشبيه بالشبكة. أظهرت الدراسة أن هذا التركيب المُركّب يُثبّت ألياف NAM في مكانها، مُشكّلًا "هالة". عندما عالج الباحثون الخلايا باللاترونكولين أ، وهو دواء يُعطّل الأكتين، اختفى تكوّن ألياف NAM وانخفضت مستويات ATP بشكل حاد.
إذا كانت الخلايا النقيلية تعتمد على انفجارات ATP المرتبطة بـ NAM، فإن الأدوية التي تعطل الهيكل يمكن أن تجعل الأورام أقل تدخلاً دون تسميم الميتوكوندريا نفسها أو التأثير على الأنسجة السليمة.
قالت الدكتورة فيرينا روبريخت، المؤلفة المشاركة في الدراسة: "إن الاستجابات الإجهادية الميكانيكية هي نقطة ضعف غير مفهومة جيدًا في الخلايا السرطانية والتي يمكن أن تفتح الباب أمام طرق علاجية جديدة".
على الرغم من أن الدراسة ركزت على الخلايا السرطانية، إلا أن الباحثين يشيرون إلى أن هذه الظاهرة على الأرجح عالمية في علم الأحياء. فالخلايا المناعية التي تمر عبر العقد اللمفاوية، وعمليات نمو الخلايا العصبية، والخلايا الجنينية أثناء التكوّن الجيني، جميعها تتعرض لإجهاد بدني مماثل.
يخلص الدكتور سديلشي إلى أنه "عندما تتعرض الخلايا للضغط، يُرجَّح أن تحمي تدفقات الطاقة إلى النواة سلامة الجينوم". ويضيف: "هذا مستوى جديد كليًا من التنظيم في بيولوجيا الخلية، ويمثل نقلة نوعية في فهمنا لكيفية تحمُّل الخلايا للإجهاد البدني".
